Neutrones, Aceleradores de PartĂculas y Radioterapia
CategorĂa de nivel principal o raĂz: Noticias y eventos
CategorĂa: Notas de prensa
Publicado: Miércoles, 24 Septiembre 2014
Imprimir
Correo electrĂłnico
ÂżCĂłmo usar aceleradores de partĂculas para generar neutrones que inducen radiaciĂłn secundarĂa empleada en radioterapia más localizada?
Â
En la actualidad, el cáncer es la segunda causa de muerte, de tal modo que se considera que a lo largo del siglo XXI llegará a ser la primera causa de mortalidad entre los paĂses desarrollados.
Â
Investigadores del Centro Nacional de Aceleradores (Universidad de Sevilla-Junta de AndalucĂa-CSIC), en colaboraciĂłn con la Universidad de Granada y otras instituciones internacionales, han llevado a cabo la medida de la secciĂłn eficaz de la reacciĂłn 33S(n,alfa)30Si en el CERN.
Â
CĂ©lulas cancerĂgenas (Wikipedia)
Â
El cáncer es una enfermedad originada por un conjunto de cĂ©lulas que crecen y se desarrollan de manera incontrolada, extendiĂ©ndose a tejidos sanos. En general, las cĂ©lulas cancerĂgenas pierden sus caracterĂsticas primitivas, invadiendo tejidos prĂłximos o incluso más alejados de la cĂ©lula original, metástasis, y creciendo y multiplicándose de un modo descontrolado.
Â
Una de las terapias empleadas para el tratamiento del cáncer es la radioterapia. Dentro de la radioterapia, existen distintas tĂ©cnicas como son la Braquiterapia, colocaciĂłn de fuentes radiactivas encapsuladas dentro del propio tumor, o la Teleterapia, uso de aceleradores de partĂculas para irradiar los tejidos cancerosos con rayos gamma, rayos X, electrones o iones de distinto tipo. A parte, existe otro tipo de radioterapia en fase de desarrollo y que aĂşn no forma parte de las terapias estándares, que se puede considerar como una combinaciĂłn de las tĂ©cnicas descritas anteriormente y llamada Captura NeutrĂłnica en Boro.
Â
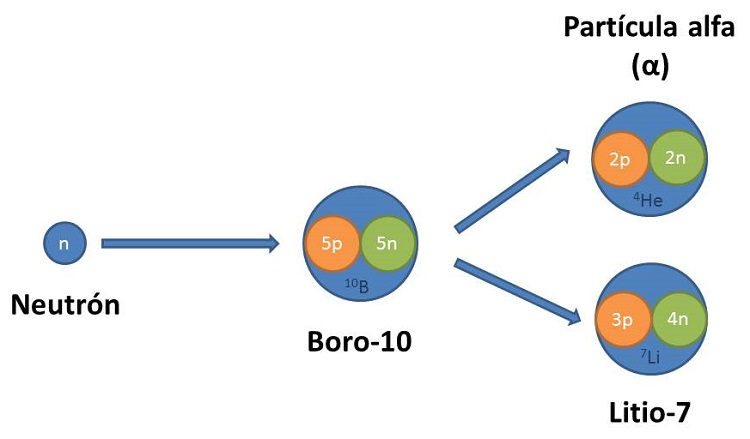
La terapia mediante Captura NeutrĂłnica en Boro o BNCT (del acrĂłnimo inglĂ©s Boron Neutron Capture Therapy) consiste en implantar un elemento, en este caso el boro-10 en las cĂ©lulas tumorales. Existen dos compuestos usados hasta ahora BPA, p-borofenilalanina, y BSH, sulfidril borano, que se absorben en las cĂ©lulas tumorales en una proporciĂłn mucho mayor que en las cĂ©lulas sanas. Para llevar a cabo esta terapia hay que irradiar con neutrones de baja energĂa la zona para producir la reacciĂłn 10B(n,alfa)7Li, es decir, se lanzan neutrones contra el boro y como consecuencia de la reacciĂłn se emiten nĂşcleos de helio (partĂculas alfa) y nĂşcleos de litio.
Â
Â
Las partĂculas alfa y 7Li son emitidas con energĂas muy altas y destruyen la cĂ©lula tumoral. Su alcance en el cuerpo humano es de pocas micras, el tamaño usual de una cĂ©lula. Como consecuencia, la acciĂłn destructiva de la radiaciĂłn es recibida casi exclusivamente por las cĂ©lulas que acumularon el boro, es decir, las cancerosas, sin dañar o con poco efecto sobre las cĂ©lulas sanas.
Â
La ventaja de esta técnica reside en que se trata de una técnica selectiva ya que el boro se fija principalmente en las células cancerosas y esto permite que el daño que provoca la radiación secundaria esté localizado fundamentalmente en el tumor con un bajo efecto en las zonas sanas.
Â
La investigaciĂłn dirigida por el Dr. Javier Praena y el Prof. Ignacio Porras ha consistido en el estudio del azufre-33 como blanco sustitutivo (o cooperativo) del boro con el fin de conocer la dosis que recibirĂa un paciente sometido a este tratamiento.
Â
Hoy en dĂa no hay estudios sobre los efectos biolĂłgicos relativos de las partĂculas alfa emitidas por el azufre-33. Sin embargo pueden ser estimados comparando con los efectos producidos por la partĂcula alfa que emite el boro-10, mediante simulaciones de Monte Carlo, o mediante experimentos que se realizarán en el CNA.
Â
El interĂ©s del uso de esta tĂ©cnica radica en que el azufre-33 en cooperaciĂłn con el boro-10, permitirĂa tratar tumores superficiales, concretamente tumores que van desde la superficie hasta una profundidad de 3 o 4 cm, y el uso de aceleradores de partĂculas para generar los neutrones. Hasta ahora los tratamientos con boro-10 se han realizado con reactores nucleares de experimentaciĂłn lo cual, entre otros, supone un problema para pacientes y equipo mĂ©dico.
Â
Los resultados del experimento realizado en el CERN por estos investigadores confirman que la reacciĂłn azufre-33(n,alfa)silicio-30 proporcionarĂa la dosis necesaria para realizar tratamientos con fuentes de neutrones basadas en acelerador.
Â
Referencia bibliográfica:
"33S as a cooperative capturer for BNCT"
"J. Praena, M. Sabaté-Gilarte, I. Porras, P.L. Esquinas, J.M. Quesada, P. Mastinu"
"Applied Radiation and Isotopes 88 (2014) 203-205"
http://dx.doi.org/10.1016/j.apradiso.2013.12.039
Visto: 5062
"33S as a cooperative capturer for BNCT"
"J. Praena, M. Sabaté-Gilarte, I. Porras, P.L. Esquinas, J.M. Quesada, P. Mastinu"
"Applied Radiation and Isotopes 88 (2014) 203-205"
http://dx.doi.org/10.1016/j.apradiso.2013.12.039
powered by social2s




 Â
 



 Â
Â